Nature综述:内行人的视角——以拟杆菌为窗口看微生物组
原创:微谨生物
发表期刊:Nature Microbiology
发表年份:2017
文章题目:An insider’s perspective: Bacteroides as a window into the microbiome
通讯作者:Andrew L. Goodman(耶鲁大学医学院)
原文链接:DOI:10.1038/nmicrobiol.2017.26
微谨生物已有拟杆菌的成熟编辑系统,可接各类拟杆菌的基因编辑项目,欢迎咨询。
人体胃肠道内栖息着极为丰富的微生物群落,构成了一个高度复杂的生态系统。过去十多年间,我们对肠道微生物群在人类健康中作用的认识迅速提升。然而,由于这些微生物群落的多样性和复杂性,研究进展受到了很大限制。更棘手的是,大多数共生微生物并非大肠杆菌或其近亲,在实验室中难以培养和操作。
幸运的是,我们肠道中一些最丰富的菌群既容易培养,又可以进行遗传操作。作为拟杆菌门中的重要菌属,专性厌氧的拟杆菌自发现以来的一百多年里,已成为人类肠道微生物学的主要研究对象。
本篇综述将以拟杆菌为窗口,深入探索肠道微生物组这一复杂世界。我们将审视使它们能够在各种环境变化或挑战中耐受和持续存在的特质,评估它们如何与邻居建立合作或对抗关系,并讨论这些共生菌与宿主之间复杂的关系——这种关系最终可能导致免疫耐受或疾病。
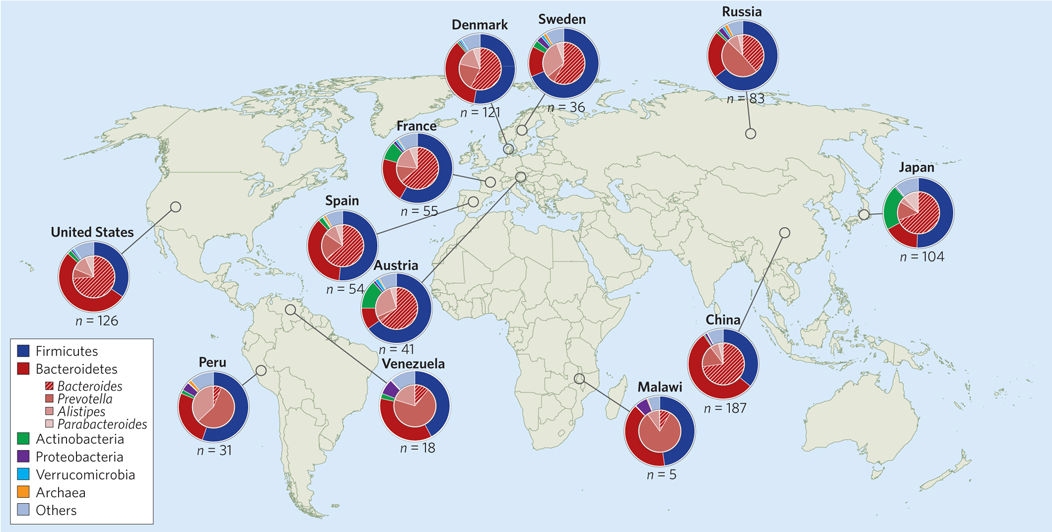
图1. 全球人群肠道微生物在门和属水平的分布与丰度
在健康成人人群中,革兰氏阳性菌厚壁菌门和革兰氏阴性菌拟杆菌门普遍存在。尽管不同人群的微生物群在门水平上可能相似(如瑞典与俄罗斯),但在更低的分类水平上往往差异显著。本图中每个饼图代表一个队列的平均值,外圈代表门水平分类,内圈代表拟杆菌门内的属水平分类。同一国家内个体间差异也很显著。
肠道微生物群落在组成上与其他自然微生物群落不同,是它们进化所处独特环境的产物。人类肠道长达7.5-8.5米,表面积超过32平方米(考虑肠绒毛后),为宿主-微生物相互作用提供了广阔空间。
为了应对各种环境挑战,拟杆菌能够主动改善肠道环境,使其对自己和其他微生物更适宜。例如,许多拟杆菌编码细胞色素bd氧化酶,可降低细胞内氧气水平,进而降低肠道氧气水平,从而允许那些原本会被氧气杀死的严格厌氧菌生长。
虽然人们可能认为肠道生活中微生物的食物选择极为丰富,但在结肠中,简单的、易于获取的糖类大多已被消耗或吸收。剩余的是复杂的、长链多糖,这些物质不能被人体酶系统消化。对于许多细菌来说,这些复杂多糖同样难以处理,无法跨膜运输。
然而,早期研究已证实拟杆菌是高效的聚糖降解者,具有识别和代谢多种植物源和宿主源多糖的特殊能力。拟杆菌通过称为多糖利用位点(PULs)的基因簇来实现这一点,这些基因簇似乎是拟杆菌门所特有的。PULs决定拟杆菌能占据哪些代谢生态位,甚至决定它们在肠道内的生物地理分布位置。
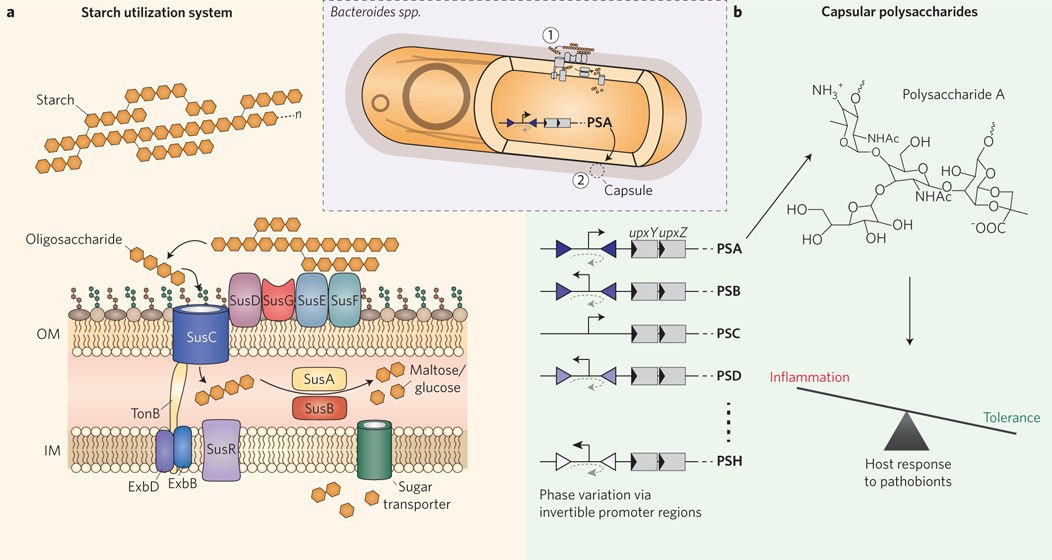
图2. 拟杆菌中多糖的消耗与生产
a, 淀粉利用系统:外膜上的淀粉结合脂蛋白(SusDEF)结合并固定大的胞外淀粉聚合物,然后由α-淀粉酶SusG将其分解为较小的寡糖。TonB依赖性转运蛋白SusC将这些寡糖转运到周质空间,随后α-淀粉酶SusA和α-葡萄糖苷酶SusB将其进一步分解为二糖(麦芽糖)或单糖(葡萄糖),通过糖转运透酶进入细胞质。周质空间中麦芽糖的存在触发调节蛋白SusR促进更多Sus组分的表达。拟杆菌基因组中通常编码80多个PULs。b, 荚膜生物合成与宿主保护:拟杆菌(如脆弱拟杆菌)的荚膜多糖生物合成受可逆启动子区域(倒三角)、反式位点抑制子(UpxZ)和顺式作用转录抗终止子(UpxY)调控。多糖A可以促进对肝螺杆菌等条件致病菌的免疫耐受,从而保护宿主免受病原体诱导的结肠炎。
比较基因组学分析已在每个拟杆菌种中鉴定出数十个不同的PUL。例如,多形拟杆菌是首个完成基因组测序的拟杆菌,其6.26 Mbp基因组中近五分之一(88个PULs)用于多糖利用。拟杆菌不是同时表达所有PUL来捕获环境中可能存在的任何多糖,而是通过多种调节机制严格调控它们的表达。
由于PUL的激活取决于肠道环境,富含植物源多糖和糖蛋白的饮食会导致PUL暂时上调以降解这些营养物。但当这些底物稀缺时(如禁食期间或某些低纤维饮食),嗜糖的拟杆菌会转换其转录谱,转而消耗宿主来源的聚糖。这些暂时性的转换可能是某些细菌在婴儿期能够定植肠道并在我们一生中持续存在的主要因素。
拟杆菌不仅擅长降解多糖,它们也组装多糖。其细胞表面覆盖着多种糖蛋白和荚膜多糖,可从细胞表面延伸数百纳米,有助于这些细菌在自然环境中的整体适应性。这些表面结构标志着微生物群落成员之间(及其宿主)的界面,因此可能在肠道微生物-微生物和微生物-宿主相互作用中发挥重要作用。
我们肠道中的微生物食物网主要建立在我们摄入的营养物之上。因此,宿主饮食在决定肠道微生物群组成中起着根本性作用,包括在婴儿期。
由于饮食与微生物群之间存在联系,人们越来越有兴趣确定可作为益生元的膳食因素,以帮助为患有炎症性肠病等疾病的患者或营养不良的婴儿促进健康的肠道微生物群。一项最近的研究分析了马拉维产后母亲的母乳,发现低水平的唾液酸化母乳低聚糖与婴儿更高程度的生长迟缓有关。
所有存在的物种中,脆弱拟杆菌和大肠杆菌对唾液酸化低聚糖表现出最强的转录反应,脆弱拟杆菌是其主要的代谢者(将唾液酸乳糖分解为唾液酸、半乳糖和葡萄糖),而大肠杆菌是这些单糖的次级消费者。令人惊讶的是,对唾液酸化低聚糖存在表现出不同转录反应的细菌中,没有一种属于双歧杆菌属——该属成员因其与人类健康的积极关联而长期被归类为益生菌。
生态相互作用在整个微生物组中很常见,群落成员会对彼此的存在和活动做出转录和代谢上的反应。使用无菌小鼠的还原论方法有助于揭示这些反应。例如,用拟杆菌门的一个代表(多形拟杆菌)和厚壁菌门的一个代表(直肠真杆菌)定植无菌小鼠,结果显示,在彼此存在的情况下,多形拟杆菌上调了某些用于分解宿主聚糖的PULs(真杆菌缺乏这些基因),而真杆菌则上调了发酵氨基酸和输入简单糖类的基因表达。
有些微生物直接依赖其他微生物获取自身无法产生的资源。最著名的是维生素B12是肠道适应性景观的核心组成部分,因为许多情况下它们对甲硫氨酸合成和其他代谢途径至关重要。几种肠道厚壁菌门、放线菌门和变形菌门通过编码从头合成这些辅因子的基因为群落其他成员提供这些辅因子。
虽然不同门的成员在肠道中确实会竞争共享资源,但更激烈的竞争似乎发生在亲缘关系较近的进化亲戚之间,它们在肠道生态系统中共享许多相同的基因和功能能力。在最极端的情况下,人肠道拟杆菌无法再次定植已携带有该物种成员的单相关无菌小鼠,表明入侵细菌的所有潜在生态位都被已建立的姐妹细胞占据。然而,一个拟杆菌种可以轻松定植已携带不同拟杆菌种的无菌小鼠,表明生态位重叠有限。
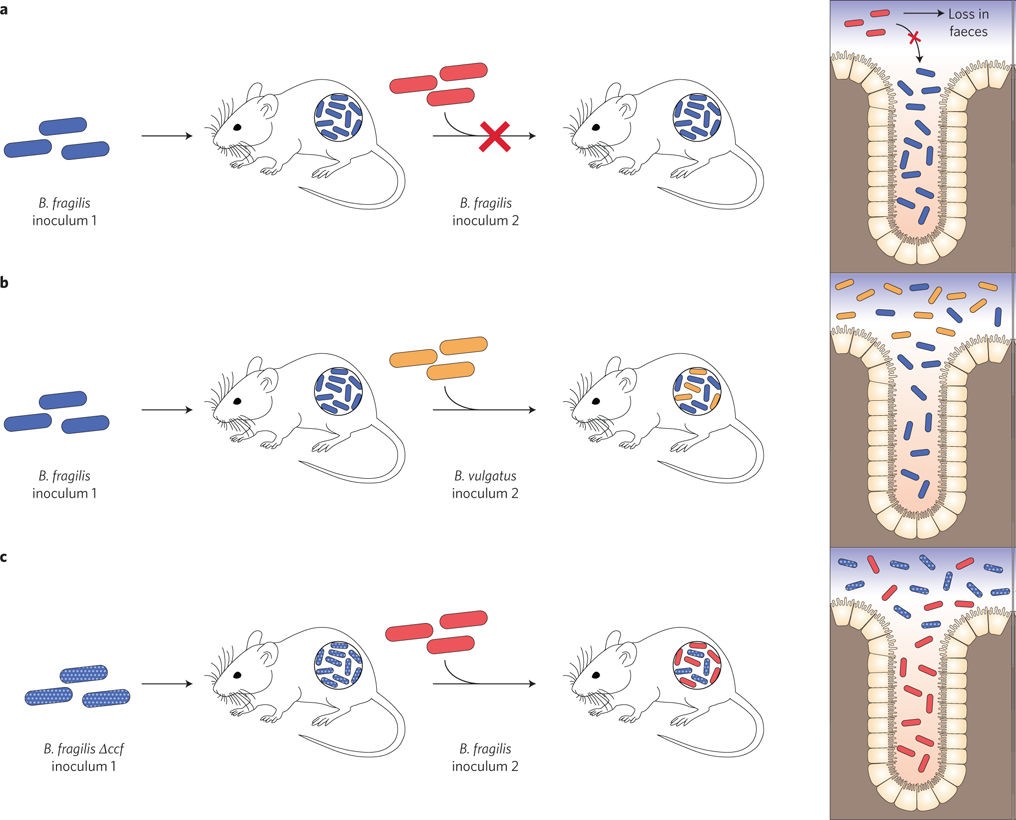
图3. 结肠隐窝的共生定植
a, 定植排斥:用脆弱拟杆菌稳定定植无菌小鼠可阻止同基因脆弱拟杆菌姐妹细胞随后的定植,表明最初的脆弱拟杆菌种群已占据其所有可用生态位,不受随机位移力的影响。b, 共定植:用脆弱拟杆菌稳定定植无菌小鼠不阻止其他拟杆菌种的入侵,表明两种菌之间生态位重叠有限。c, 生态位位移:用缺乏称为共生定植因子(CCF)的特殊PUL基因的脆弱拟杆菌突变体稳定定植无菌小鼠后,可被随后定植的野生型脆弱拟杆菌细胞破坏。脆弱拟杆菌CCF突变体在定植结肠隐窝深处方面存在缺陷,隐窝被认为是播撒肠腔并促进肠道长期定植的微生物储存库。
肠道中合作者和竞争者之间的界限远非清晰,许多物种似乎同时扮演着两种角色。例如,我们知道一些拟杆菌种在共培养实验中会竞争膳食多糖,但又通过分泌外膜囊泡(OMVs)或通过细胞本身锚定的酶的胞外活性,与邻近物种分享它们部分的多糖获取机制。令人惊讶的是,这些OMV可以作为公共物品在微生物群遗传上不同的成员之间穿梭,从而使其他物种能够扩展其碳源范围,而无需直接编码相关基因。
然而,肠道微生物之间的一些相互作用似乎是纯粹对抗性的,甚至是领土性的,通过分泌毒性蛋白来实现。细菌素是可自由扩散的分泌毒素,具有多种催化功能,包括孔形成、核酸降解和抑制细胞壁合成,通常由亲缘关系密切的菌株和种产生,也以它们为靶标。
肠道中的高细菌密度可能会显著增强邻近细胞之间的资源竞争。许多肠道拟杆菌门似乎找到了减少非遗传同一细胞之间对共享资源的局部竞争的方法,部分是通过使用VI型分泌系统(T6SSs)。这些多蛋白机器在直接细胞接触后,迅速将称为效应物的抗菌毒素注入邻近细胞。拟杆菌门的T6SS在进化上不同于研究较深入的变形菌门的T6SS,并共同分为三种不同的结构类型。
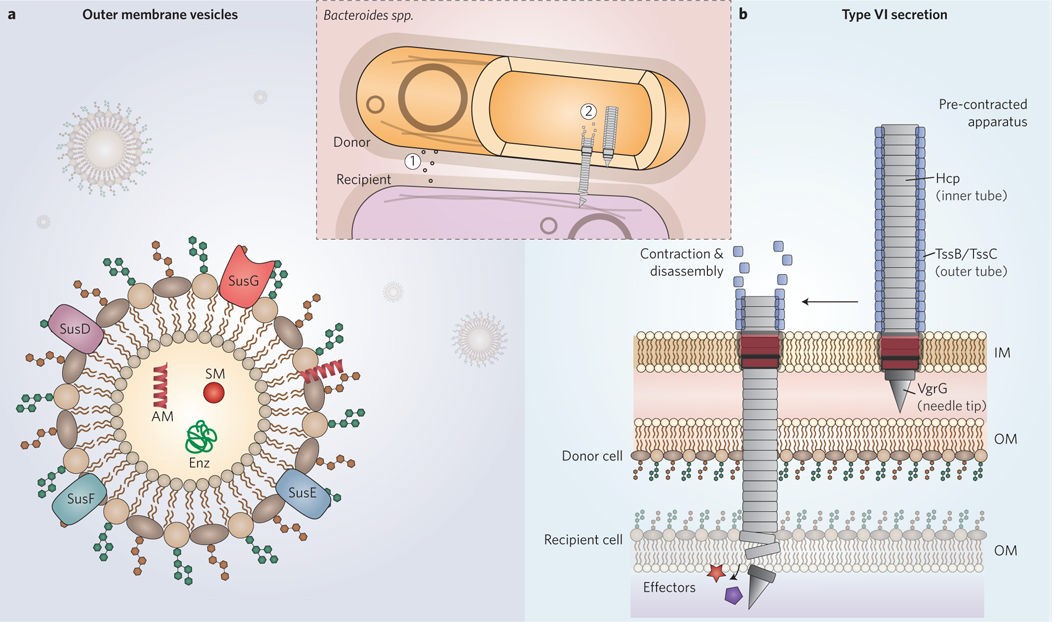
图 4. 拟杆菌属细菌间合作与拮抗的机制
a, 外膜囊泡(OMVs):OMVs由拟杆菌在体内外产生和释放。它们可作为公共物品的载体,包括Sus-like组分、小分子辅因子、抗炎荚膜组分(如PSA)、抗菌蛋白(如BSAP-1)和其他酶类。b, 拟杆菌门VI型分泌系统(T6SS):细菌T6SS是一种可收缩的分子注射器,能以细胞间接触依赖的方式将毒性效应蛋白快速递送到邻近细胞。由TssB/TssC多聚体组成的外管处于高能状态,收缩至低能状态,迫使由Hcp多聚体组成的内管从供体细胞射出并进入附近受体细胞。针尖可携带结合的效应蛋白,在缺乏同源免疫蛋白的易感受体细胞中介导细胞损伤和死亡。
人类胃肠道与微生物持续接触。总的来说,这些微生物对宿主免疫系统产生深远影响,无论是在病原体感染的背景下,还是在炎症性肠病、癌症或自身免疫疾病中。在很大程度上,微生物群中友敌的区分取决于这些与宿主免疫的相互作用,且通常取决于宿主内生物地理学位置、微生物群组成和某些营养物可用性等多种外在因素。拟杆菌展示了一个细菌群体如何能戴上三顶不同的帽子——共生菌、互生菌甚至条件致病菌。
肠道微生物群对免疫系统发育的影响,或许最明显地体现在对比常规动物和无菌动物的研究中。无菌动物不仅免疫系统发育不全,而且更容易受到肠道病原体的感染。用拟杆菌定植无菌小鼠纠正了这些免疫缺陷中的许多方面,表明拟杆菌与宿主之间存在重要的相互作用。
拟杆菌的其他表面结构也显示出具有免疫调节作用。一项研究将爱沙尼亚和芬兰儿童中1型糖尿病的患病率与它们相对较高的拟杆菌丰度联系起来,相比之下俄罗斯儿童的1型糖尿病患病率低且双歧杆菌丰度较高。通过体外试验和动物模型,他们证明了芬兰受试者中最主要的拟杆菌种——多氏拟杆菌的脂多糖(LPS)能促进免疫耐受,且与大肠杆菌的LPS相比,未能保护非肥胖糖尿病小鼠免于发展自身免疫性糖尿病。
尽管拟杆菌揭示了微生物在促进健康方面的重要作用,但这些物种也与重要的人类疾病有关。肠道病原体肠出血性大肠杆菌(EHEC)已知会在肠上皮形成附着和抹平损伤,导致严重腹泻。令人惊讶的是,它的致病性被其他有益的微生物增强,例如肠道共生菌多形拟杆菌和普通拟杆菌,它们从粘膜糖蛋白上切割下岩藻糖、唾液酸和其他糖类,然后被EHEC消耗,导致其毒力基因表达增强。
使微生物群与宿主组织保持接触的粘膜屏障至关重要,在某些情况下可能受损,包括肠道手术、克罗恩病或溃疡性结肠炎引起的组织损伤、憩室炎发展或阑尾破裂。当这种情况发生时,患者发生腹腔内脓肿的风险更高,必须引流并用抗生素治疗。一个多世纪前的研究就注意到,从脓肿中分离出的厌氧菌远比需氧菌丰富。
为了持续存在,我们的肠道微生物必须能够经受住炎症期。发炎肠道内的主要因素包括分泌的宿主抗菌因子,例如靶向肽聚糖的凝集素RegIIIγ和靶向LPS的肽hLL-37。由于许多抗菌肽带正电荷,它们被吸引到革兰氏阴性菌带负电的外膜上,从而介导细胞损伤。在进化史上,拟杆菌通过直接修饰其LPS变得高度抵抗宿主抗菌肽。
人类肠道微生物组巨大的生物复杂性给科学界带来了艰巨的挑战,并对我们精确研究、理解和操纵这些群落的能力造成了诸多障碍。进展的主要障碍之一是缺乏合适的遗传工具来剖析我们的微生物,以确定它们在细胞和分子水平上是如何工作的。
由于拟杆菌属的成员可培养且易于遗传操作,它们已成为理想的人类肠道细菌模型群体。数十年来研究拟杆菌所获得的经验,可以帮助我们理解肠道微生物群的其他成员及其对宿主健康的影响。
理解拟杆菌如何避免触发宿主免疫通路或逃避抗菌分子的攻击,它们如何分解来自食物颗粒或宿主粘液的营养物,它们如何响应宿主饮食的变化和其他扰动,或者它们如何彼此及与群落其他成员相互作用,最终可能为我们指明肠道微生物生理学的基本潜在机制。扎实掌握这些基本原理,可能使我们在开发靶向疗法方面取得巨大进步,通过改变患者的微生物群来对抗与肠道微生物群相关的多种疾病、感染和紊乱。
拟杆菌作为人类肠道微生物组的核心成员,经过一个多世纪的研究,已经为我们理解肠道微生物的生物化学、生态学和与宿主的相互作用提供了宝贵的窗口。从多糖利用系统(PULs)到荚膜多糖的相变调节,从VI型分泌系统(T6SS)介导的菌间竞争到免疫调节分子PSA,拟杆菌的研究不断揭示着肠道微生物组的运作原理。随着研究的深入,拟杆菌不仅在基础科学层面为我们提供了重要见解,在应用层面也为开发新一代益生菌和治疗策略带来了新思路。理解拟杆菌如何与宿主和其他微生物互作,将为调控肠道稳态、预防和治疗相关疾病奠定重要基础。
主要参考文献:
[1] Sender R, Fuchs S, Milo R. Cell. 2016; 164:337-340.
[2] Gill SR, et al. Science. 2006; 312:1355-1359.[3] Ley RE, et al. Science. 2008; 320:1647-1651.
[4] Martens EC, Chiang HC, Gordon JI. Cell Host Microbe. 2008; 4:447-457.
[5] Comstock LE, Kasper DL. Cell. 2006; 126:847-850.
[6] Mazmanian SK, Round JL, Kasper DL. Nature. 2008; 453:620-625.
[7] Russell AB, et al. Cell Host Microbe. 2014; 16:227-236.
[8] Goodman AL, et al. Cell Host Microbe. 2009; 6:279-289.
[9] Cullen TW, et al. Science. 2015; 347:170-175.
[10] Vatanen T, et al. Cell. 2016; 165:842-853.
