ACS Synthetic Biology丨开发适用于人类肠道共生拟杆菌的CRISPR/Cas基因组编辑工具
原创:微谨生物
发表期刊:ACS Synthetic Biology
发表年份:2022
文章题目:CRISPR/Cas-Based Genome Editing for Human Gut Commensal Bacteroides Species
通讯作者:戴磊 研究员(中国科学院深圳先进技术研究院)
原文链接:DOI 10.1021acssynbio.1c00543
微谨生物已有拟杆菌的成熟编辑系统,可接各类拟杆菌的基因编辑项目,欢迎咨询。

人体肠道内栖息着极为丰富的微生物群落,其中拟杆菌属是人类肠道微生物组中丰度最高的菌属,在维持健康的肠道微生态中发挥着重要作用。拟杆菌与多种疾病密切相关,如肥胖、炎症性肠病和结直肠癌,同时它们也被越来越多地用作模型生物,研究肠道共生菌的生理功能,例如多糖利用位点、致病机制、胆汁酸代谢以及肠道微生物组的生态与进化。
然而,目前针对拟杆菌的遗传操作工具仍十分有限。现有的基因编辑方法存在诸多局限性:基于NBU元件的插入方法只能在特定基因组位点进行整合,且无法实现无痕编辑;等位交换方法虽然常用,但编辑效率不高。因此,开发高效、通用的拟杆菌基因组编辑工具,对于功能解析肠道微生物组具有重要价值。
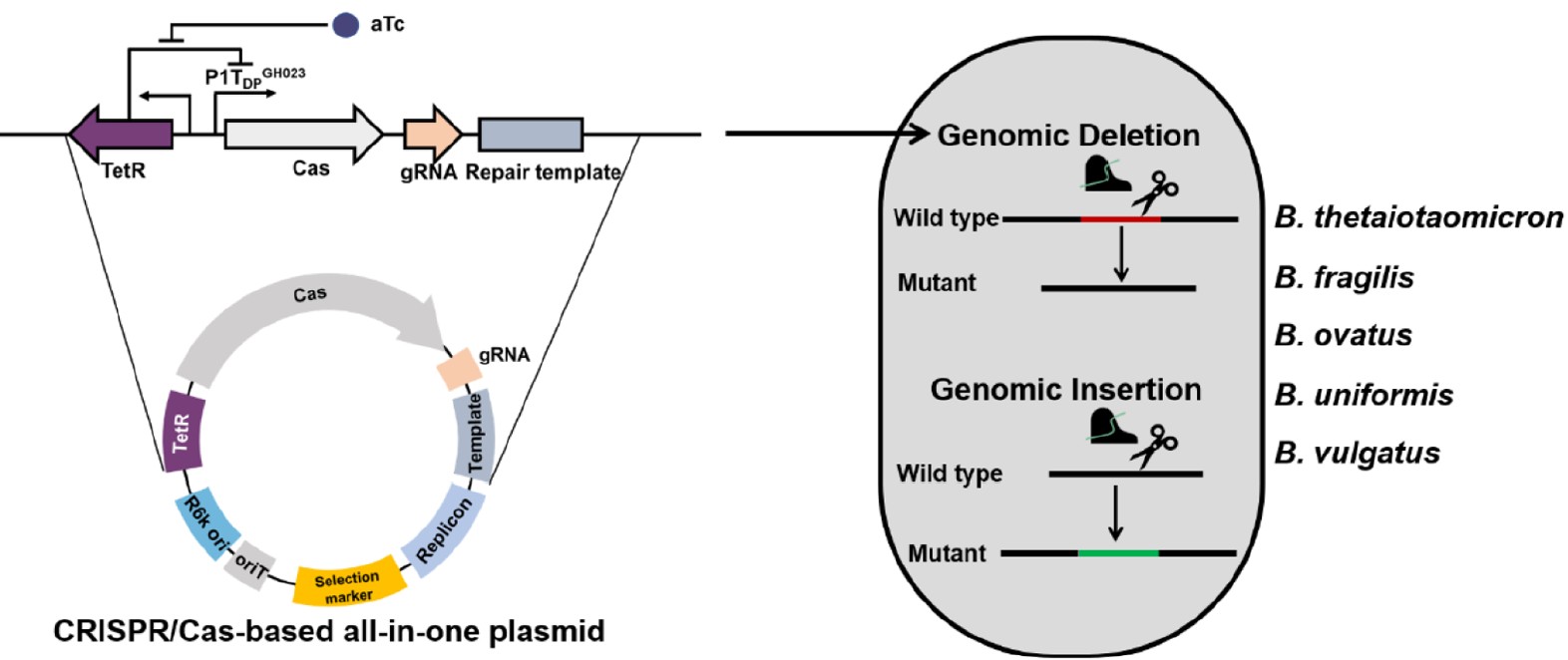
TOC
本研究系统评估了三种不同的CRISPR/Cas系统(FnCas12a、SpRY和SpCas9)在多形拟杆菌中的编辑效率,成功开发了一种高效、无痕的CRISPR/Cas基因组编辑工具,并验证了其在多种拟杆菌物种中的广泛适用性。
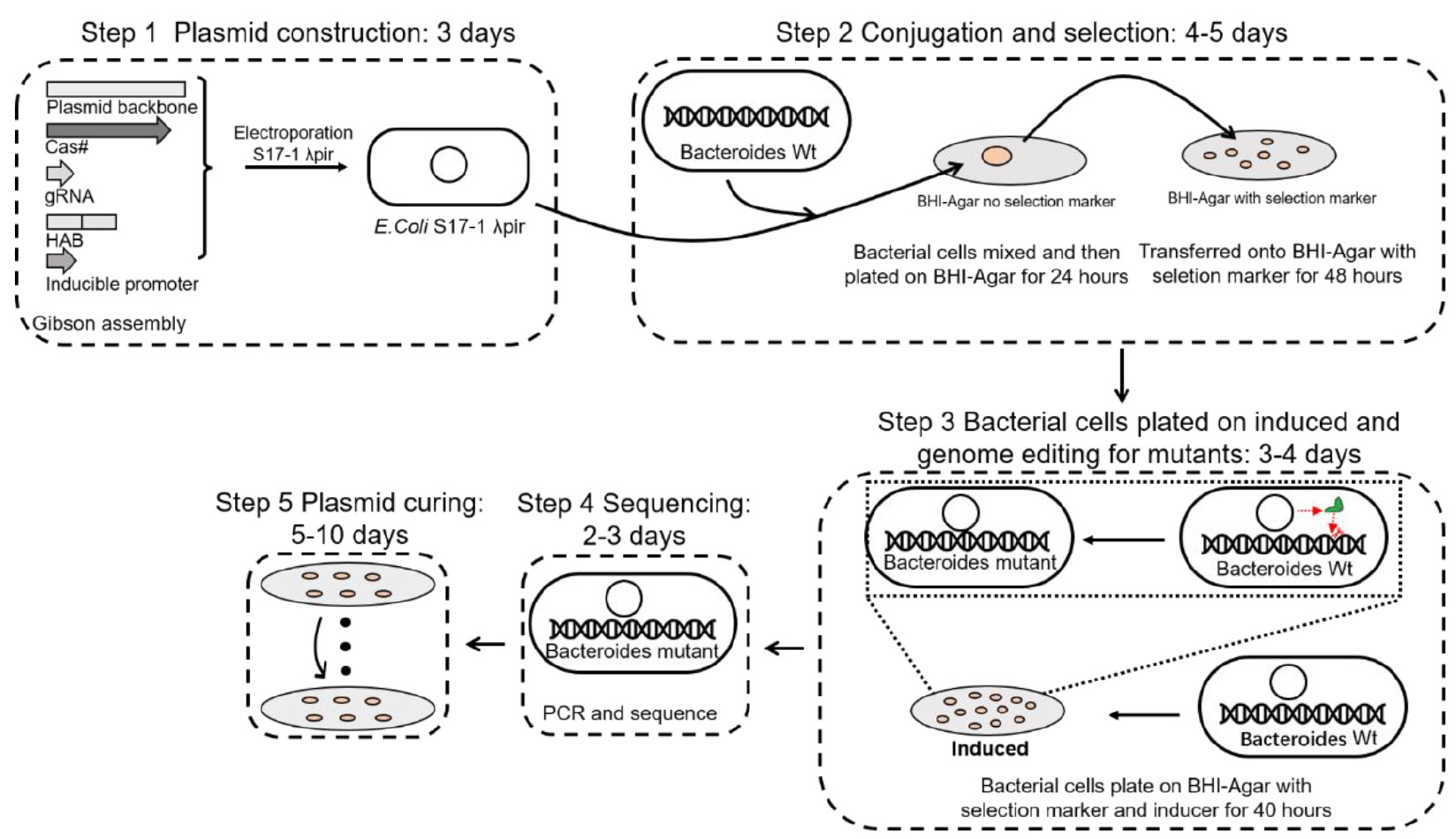
图1. CRISPR/Cas基因组编辑在拟杆菌中的工作流程
本研究开发了一套一体化的CRISPR/Cas基因组编辑系统,实验流程分为五个步骤:第一步,利用Gibson组装方法构建多形拟杆菌-大肠杆菌穿梭质粒;第二步,将质粒接合转移至拟杆菌中,通过筛选标记分离转化子;第三步,诱导Cas蛋白表达,激活基因编辑过程;第四步,通过PCR和测序验证拟杆菌突变体;第五步,将突变体菌株在不含抗生素的培养基中培养,进行质粒消除。
这一流程实现了从质粒构建到突变体验证的完整闭环,为拟杆菌的遗传操作提供了系统性的技术方案。
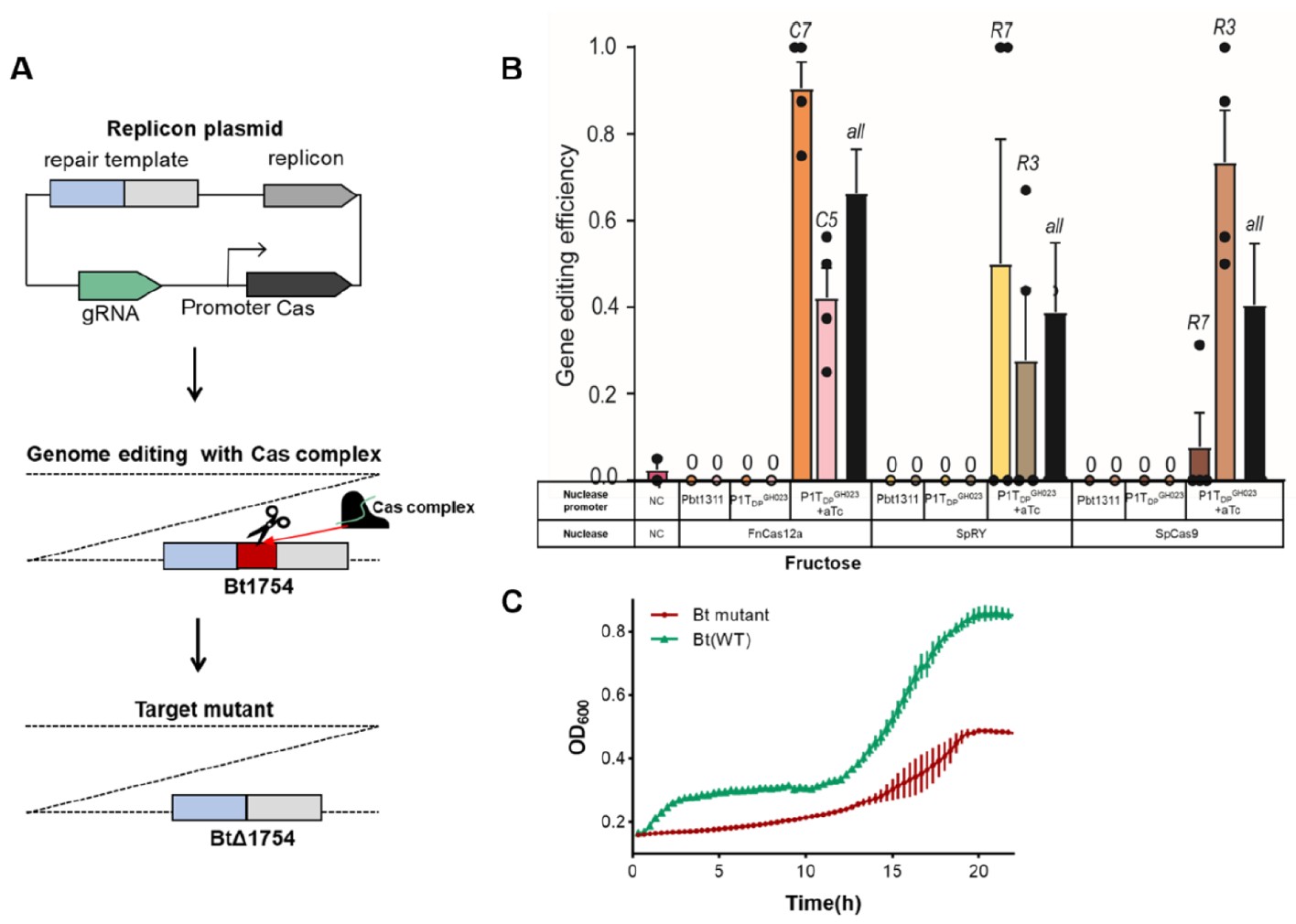
图2. 多形拟杆菌中CRISPR/Cas基因组编辑系统的评估
为了确定哪种CRISPR/Cas系统具有最高的编辑效率,研究人员设计了一系列一体化质粒,以Bt1754基因为靶点进行基因删除实验。Bt1754是多形拟杆菌中利用果糖所必需的基因。
结果显示,当Cas蛋白受组成型启动子Pbt1311控制时,未能获得任何突变体;而当Cas蛋白受诱导型启动子P1TDPGH023控制时,在aTc诱导下,FnCas12a、SpRY和SpCas9的编辑效率分别达到约60%、40%和40%。这表明诱导型CRISPR/Cas系统可用于人肠道拟杆菌的基因组编辑,其中FnCas12a的效率最高。
通过对野生型和BtΔ1754突变体在果糖培养基中的生长曲线测定,进一步验证了基因编辑的成功。
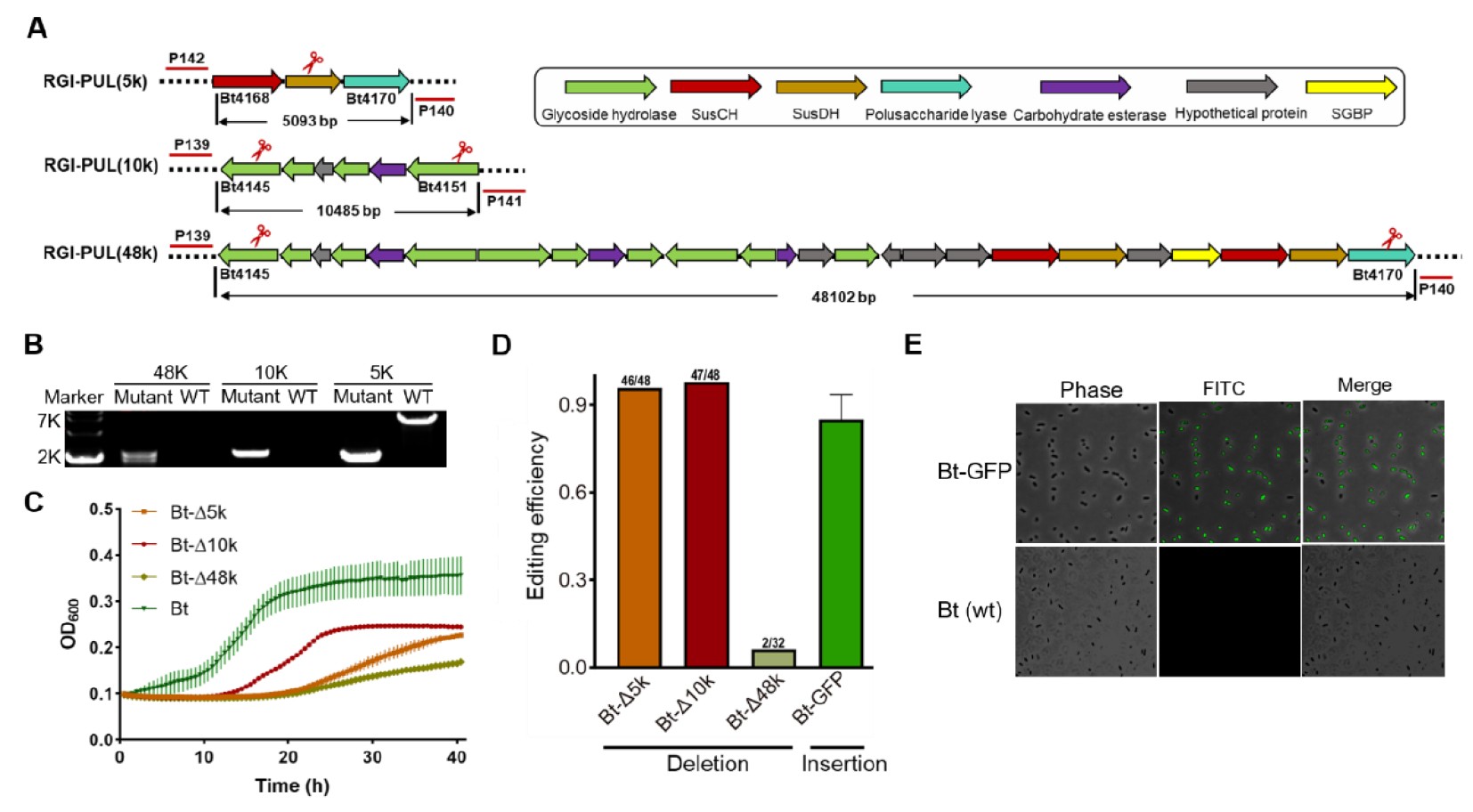
图3. 利用CRISPRFnCas12a系统在多形拟杆菌中实现无痕基因组编辑
基因簇如多糖利用位点(PULs)是理解肠道微生物组代谢功能和代谢介导的生态互作的关键。然而,现有的肠道共生菌编辑工具很难实现大片段基因组区域的靶向删除。
研究人员选择参与鼠李糖半乳糖醛酸聚糖-I利用的PUL(RGI-PUL)作为目标,进行了三种不同大小的片段删除:5 kb、10 kb和48 kb。结果显示,所有三个片段均被成功删除,其中5 kb和10 kb片段的删除效率接近100%,48 kb片段的效率约为6%。删除突变体在以鼠李糖半乳糖醛酸聚糖为唯一碳源的培养基中,生长速率呈现不同程度的下降。
此外,研究人员还成功在Bt1754位点插入了绿色荧光蛋白基因gfp,插入效率超过80%。荧光显微镜观察证实,改造后的菌株成功表达了GFP。
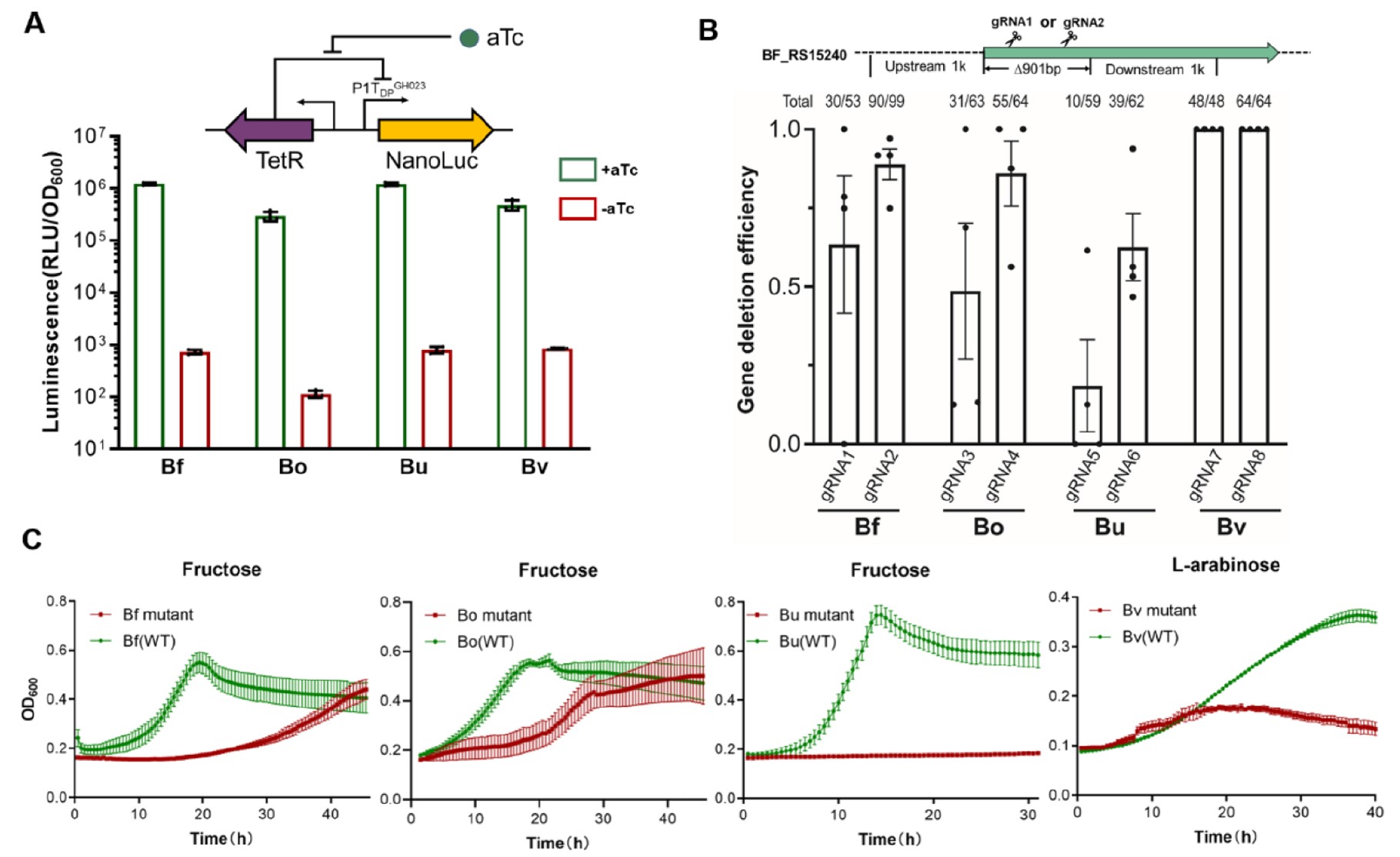
图4. CRISPRFnCas12a基因组编辑系统在多种拟杆菌物种中的应用
为了验证该系统是否适用于不同的人肠道共生拟杆菌物种,研究人员构建了一套用于改造脆弱拟杆菌、卵形拟杆菌、普通拟杆菌和单形拟杆菌的一体化质粒。
首先评估了aTc诱导型启动子在不同拟杆菌物种中的活性,结果显示该系统在多个物种中均有良好的诱导表达。针对每个物种的特定基因进行删除实验,编辑效率均在40%以上。通过对野生型和突变体菌株在不同碳源培养基中的生长曲线测定,进一步验证了编辑的成功。
这表明CRISPRFnCas12a系统可广泛应用于多种人肠道拟杆菌物种的遗传改造。
总结与展望
本研究成功开发了一种高效、无痕的CRISPR/Cas基因组编辑工具,适用于多种人肠道拟杆菌物种。研究团队系统评估了不同Cas蛋白(FnCas12a、SpRY、SpCas9)和启动子(组成型、诱导型)的编辑效率,发现诱导型CRISPRFnCas12a系统具有最高的编辑效率。利用这一系统,研究人员成功实现了高达50 kb的大片段基因组删除和GFP基因的靶向插入,并在五种拟杆菌物种中验证了其广泛适用性。
这一工具的开发为拟杆菌的功能研究和工程化改造提供了重要的技术支撑。随着合成生物学的发展,改造肠道共生菌作为工程化活体生物药用于治疗人类疾病展现出广阔前景。CRISPR/Cas基因组编辑工具的问世,将极大地促进肠道共生菌的机制研究和活体生物药的开发。
主要参考文献:
[1] Wexler AG, Goodman AL. An insider's perspective Bacteroides as a window into the microbiome. Nat Microbiol. 2017; 217026.
[2] Liu R, et al. Gut microbiome and serum metabolome alterations in obesity and after weight-loss intervention. Nat Med. 2017; 23859-868.
[3] Brown EM, et al. Bacteroides-derived sphingolipids are critical for maintaining intestinal homeostasis and symbiosis. Cell Host Microbe. 2019; 25668-680.
[4] Mimee M, et al. Programming a human commensal bacterium, Bacteroides thetaiotaomicron, to sense and respond to stimuli in the murine gut microbiota. Cell Syst. 2015; 162-71.
[5] Taketani M, et al. Genetic circuit design automation for the gut resident species Bacteroides thetaiotaomicron. Nat Biotechnol. 2020; 38962-969.
