Scientific Reports丨利用源自植物乳杆菌的锚定序列在多种乳杆菌属物种中实现异源蛋白的表面展

原创:微谨生物
发表期刊:Scientific Reports
发表年份:2020
文章题目:Anchoring of heterologous proteins in multiple Lactobacillus species using anchors derived from Lactobacillus plantarum
通讯作者:Geir Mathiesen 教授(挪威生命科学大学)
原文链接:DOI 10.1038/s41598-020-66515-7
乳杆菌属包含200多个物种,在食品、生物技术和治疗应用中具有重要的经济价值。乳杆菌在人类应用中有着悠久的安全使用历史,被公认为GRAS(一般认为安全)状态。由于乳杆菌是安全的且可能具有免疫刺激佐剂效应,它们是递送抗原和其他医用分子的理想载体。
理想情况下,抗原应在胃肠道严酷环境中受到保护免受蛋白酶解损伤,同时在粘膜表面充分暴露以激发有利的免疫反应。分泌释放的抗原容易被降解,而嵌入细胞壁的抗原可能得到更好的保护但免疫系统可及性较差。因此,在设计表达系统时,仔细考虑抗原的亚细胞定位至关重要,因为细菌表面不同的定位将导致不同的免疫反应。
本研究评估了三种源自植物乳杆菌的表面锚定序列,用于在多种乳杆菌属物种中实现蛋白质表面展示。研究以结核分枝杆菌杂交抗原Ag85B-ESAT-6(简称AgE6)为测试蛋白,测试了脂蛋白锚定、LPXTG基序介导的共价细胞壁锚定和LysM结构域介导的非共价细胞壁锚定三种策略,在八种乳杆菌中的展示效果。
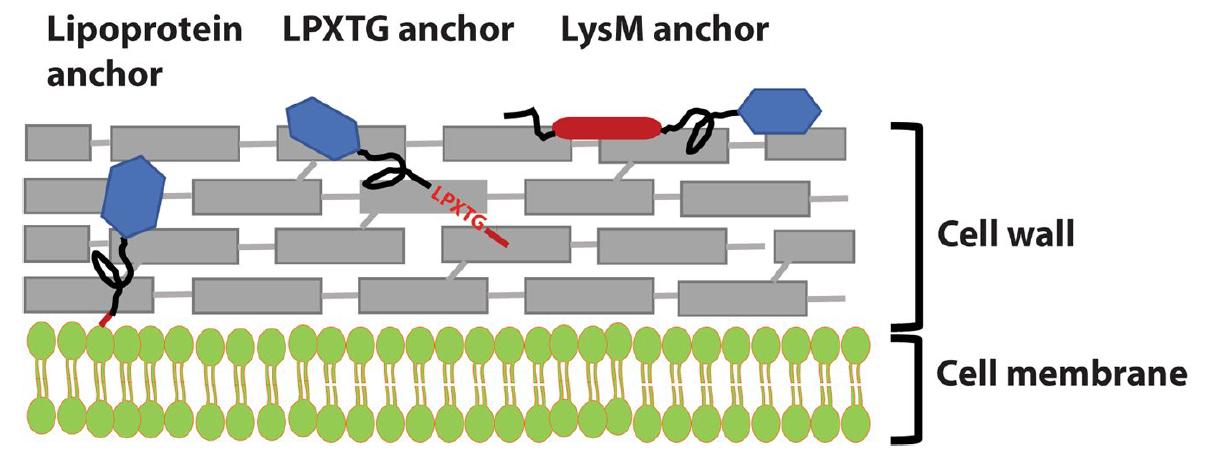
图1. 三种锚定策略的示意图
红色表示各种锚定结构域和基序,黑色表示锚定序列与融合抗原之间的连接区域,蓝色表示抗原。a脂蛋白锚定:通过信号肽酶II切割并在N端半胱氨酸上偶联脂质,使蛋白与细胞膜结合。b LPXTG共价细胞壁锚定:分选酶切割LPXTG基序并将苏氨酸残基共价连接到肽聚糖层。c LysM非共价细胞壁锚定:LysM结构域特异性结合细胞壁中的N-乙酰葡糖胺残基。
此前已有研究表明,使用不同的锚定类型(可能导致展示蛋白的不同定位)会影响下游免疫反应。不同的乳杆菌物种具有不同的表面结构,这可能影响锚定蛋白的表面暴露程度以及免疫调节效应。此外,乳杆菌物种在展示抗原的数量上也可能存在差异,这同样会影响下游反应。
例如,一项先前的研究在植物乳杆菌、短乳杆菌、加氏乳杆菌和罗伊氏乳杆菌中表达了脂蛋白锚定的结核抗原AgE6,结果显示这些重组菌株在小鼠中诱导了明显不同的免疫反应。体外研究也表明,这四种物种能够激活人树突状细胞,而树突状细胞激活对于疫苗的T细胞反应至关重要。
因此,在开发基于乳杆菌的疫苗时,值得探索不同的表面锚定序列以及不同的乳杆菌物种。本研究旨在评估源自植物乳杆菌的三种不同表面锚定序列,在八种乳杆菌属物种中靶向结核分枝杆菌杂交抗原的效果。
表1. 本研究中使用的菌株
| 菌株 | 特征来源 |
|---|---|
| 乳酸乳球菌 IL1403 | 亚克隆宿主菌 |
| 植物乳杆菌 WCFS1 | 人唾液,分泌宿主 |
| 短乳杆菌 DSM20556 | 绿橄榄,分泌宿主 |
| 鼠李糖乳杆菌 GG | 人胃肠道,分泌宿主 |
| 弯曲乳杆菌 DSM 20019 | 牛奶,分泌宿主 |
| 加氏乳杆菌 ATCC 33323 | 人胃肠道,分泌宿主 |
| 清酒乳杆菌 LB790 | 肉制品,分泌宿主 |
| 罗伊氏乳杆菌 DSM 20016 | 人胃肠道,分泌宿主 |
| 嗜酸乳杆菌 ATCC 4356 | 人胃肠道,分泌宿主 |
研究人员基于pSIP表达系统构建了三种锚定载体。为了扩大宿主范围,研究团队使用广宿主范围复制子SH71替换了原有的窄宿主范围复制子256rep,从而使载体能够在所有八种测试乳杆菌中复制传代。
通过Western blot检测诱导后3小时的细胞裂解液,使用抗ESAT-6抗体进行检测。结果显示,所有预期产生抗原的菌株中均检测到AgE6的存在,主条带出现在预期位置。融合蛋白的预期大小因锚定序列长度不同而异:胞内表达约41 kDa,脂蛋白锚定约48 kDa,LPXTG锚定约69 kDa,LysM锚定约66 kDa。额外的条带可能是由于靶蛋白的蛋白水解降解所致,这在细胞应激时常见。条带强度在不同菌株和锚定类型之间存在差异,表明生产水平存在差异。
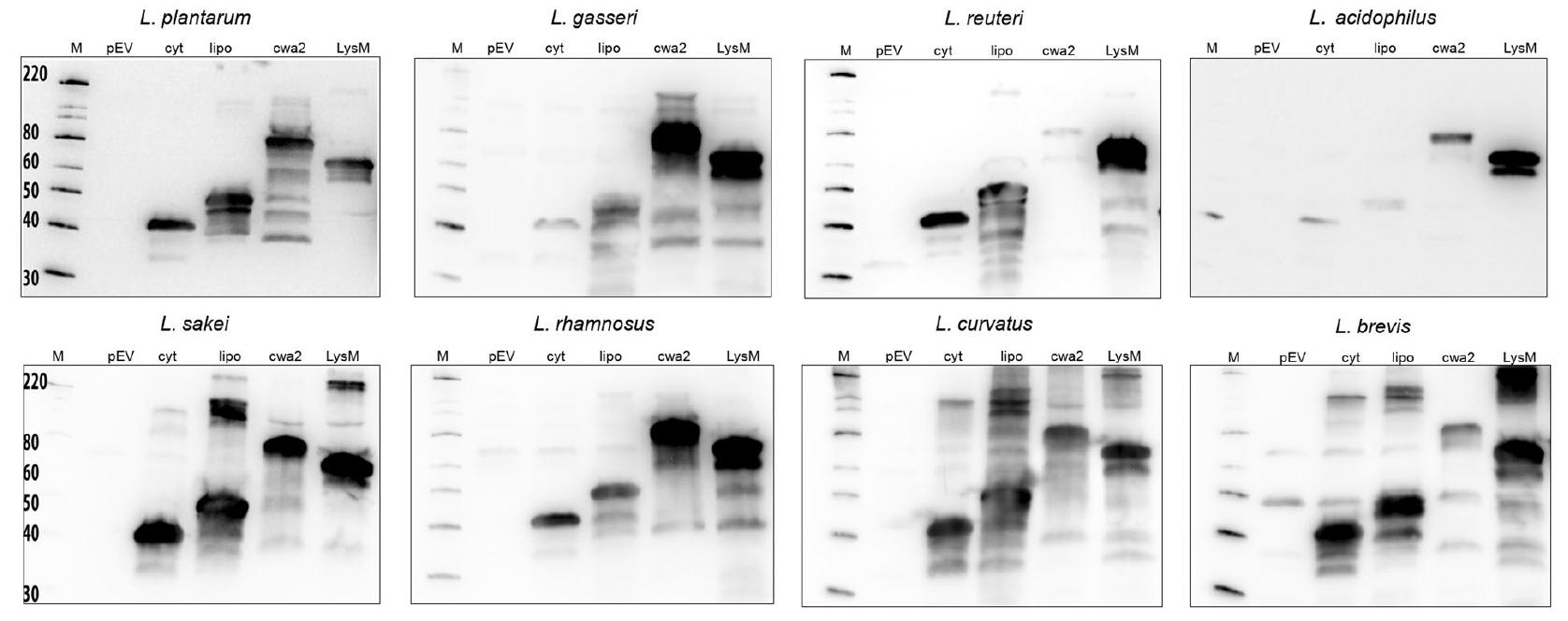
图2. 抗原的生产情况
Western blot检测AgE6-DC表达菌株诱导后3小时的细胞裂解液。样品量根据收获时OD₆₀₀进行调整,所有样品代表大致等量的细胞。泳道:M,分子量标记;pEV,空载体菌株;cyt,胞内表达载体菌株;lipo、cwa2和LysM,携带不同锚定质粒的菌株裂解液。结果显示所有预期菌株均产生抗原,但产量存在差异。
为了检测异源蛋白过度表达对宿主的影响,研究人员测量了重组菌株的生长曲线。结果显示,分泌型蛋白的生产普遍降低了生产菌株的生长速率。相比之下,胞内生产AgE6几乎没有降低生长速率,这表明对生长的负面影响主要与转运系统的过载有关,可能诱导应激反应,导致生长迟缓和蛋白降解。这在一些重组植物乳杆菌、清酒乳杆菌和弯曲乳杆菌中尤为明显,诱导导致生长严重受损。
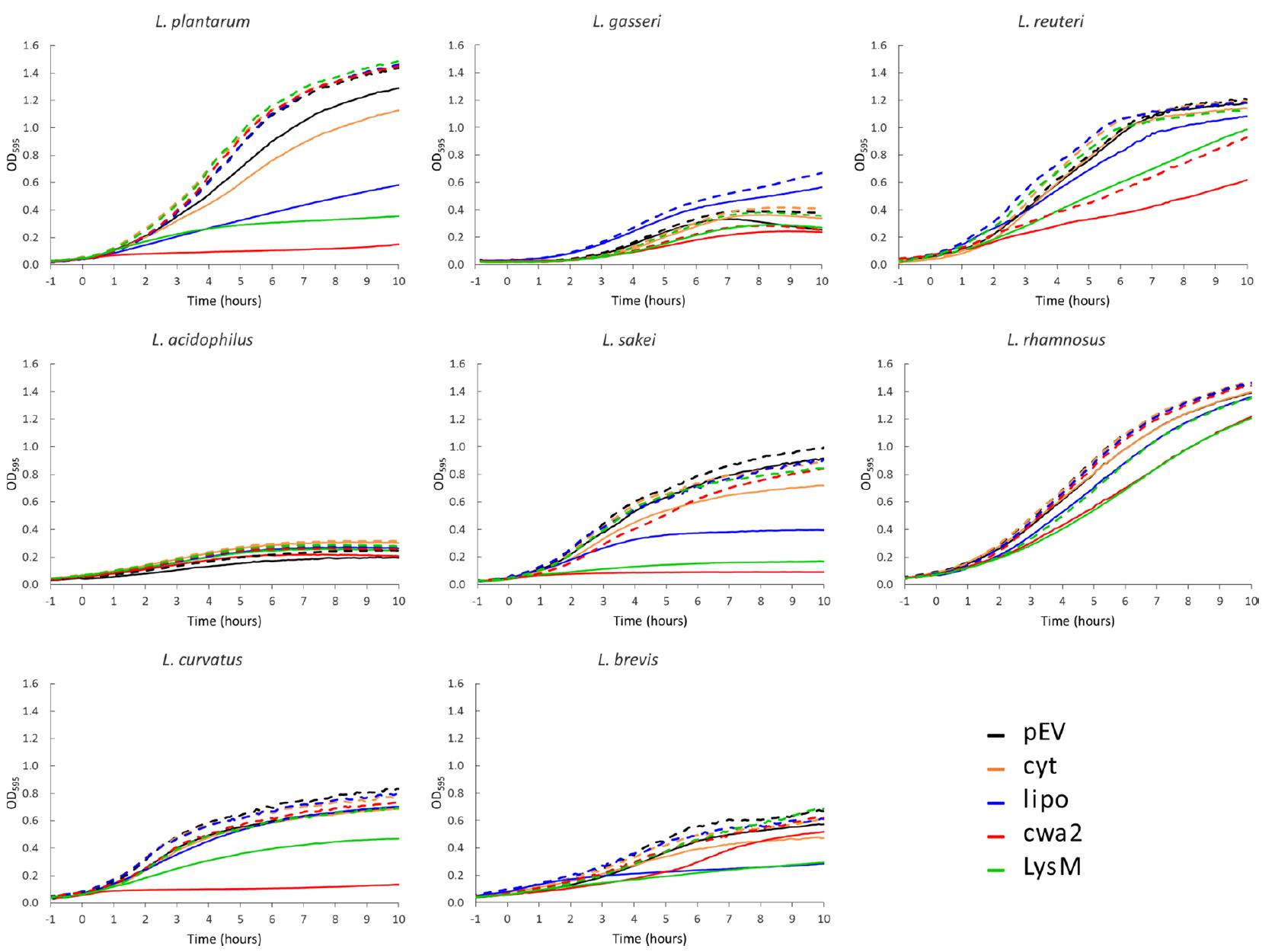
图3. 重组乳杆菌菌株的生长曲线
携带胞内表达(cyt)或表面展示(lipo、cwa2、LysM)AgE6-DC质粒的乳杆菌,以及携带空载体(pEV)的菌株,在诱导(实线)或不诱导(虚线)基因表达条件下的生长曲线。结果显示,分泌型抗原的表达普遍降低生长速率,而胞内表达影响较小。
为了验证AgE6锚定蛋白的表面定位,研究人员使用流式细胞术进行分析。结果显示,对于预期通过LPXTG和LysM基序锚定到细胞壁的菌株,大多数细菌的荧光信号较阴性对照(pEV)明显增强。
嗜酸乳杆菌未检测到表面展示,尽管Western blot证实了两种杂交蛋白的生产。一种可能的解释是源自植物乳杆菌的Lp_3050信号肽在嗜酸乳杆菌中无功能。众所周知,异源蛋白的分泌效率可能因信号肽的选择而受到显著影响。
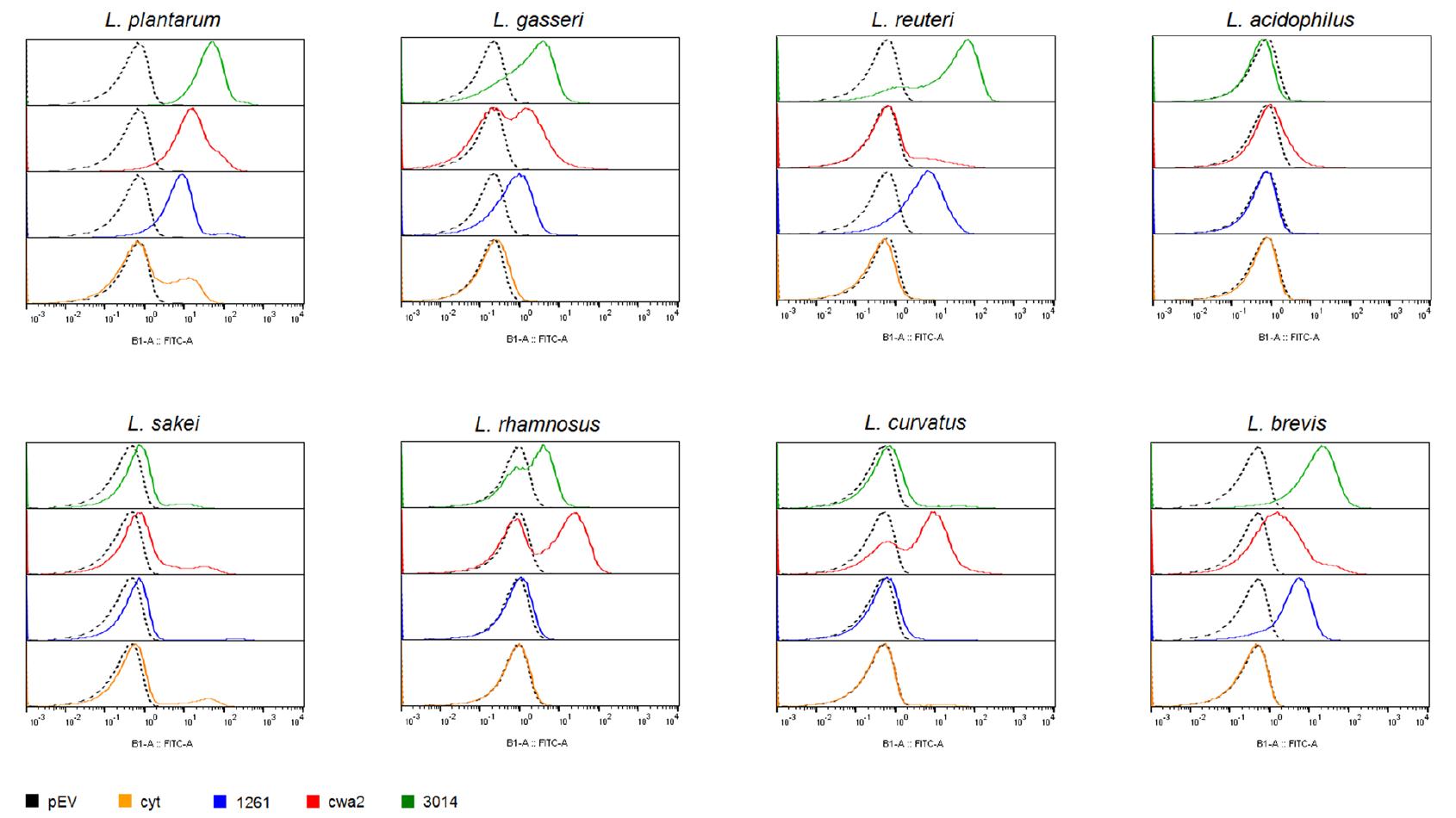
图4. 八种乳杆菌中AgE6-DC表面展示的流式细胞术分析
诱导后3小时收获细胞。pEV,空载体菌株(黑色虚线);cyt,胞内表达载体菌株(黄色);lipo(蓝色)、cwa2(红色)和LysM(绿色),携带不同表面锚定表达质粒的菌株。结果显示,除嗜酸乳杆菌外,其他菌株均检测到不同程度的表面展示信号。
免疫荧光显微镜分析证实了七种重组菌株的细胞壁锚定AgE6表面暴露。值得注意的是,信号强度在阳性菌株之间以及两种锚定方式之间存在差异,这可能是由于分泌和锚定水平不同,和/或细胞壁结构差异导致检测抗体的可及性不同。
植物乳杆菌作为LPXTG和LysM锚定序列的来源菌株,在流式细胞术和荧光显微镜中均显示强信号,表明使用同源分泌和锚定信号可能更有利。
流式细胞术数据和免疫荧光显微镜均显示抗原展示细胞群体内存在异质性。流式数据有时显示双峰分布,表明存在两个细菌群体,特别是对于cwa2菌株。显微镜也显示有色和无色细胞的混合。这种异质性可能反映了细胞生长阶段的差异,这可能影响展示抗原的数量或对抗体的可及性。

图5. 免疫荧光显微镜分析AgE6-DC表面展示(一)
诱导后3小时收获细胞。pEV,空载体菌株;cyt,胞内表达载体菌株;lipo、cwa2和LysM,携带不同表面锚定表达质粒的菌株。结果显示植物乳杆菌、加氏乳杆菌、罗伊氏乳杆菌和嗜酸乳杆菌的表面展示情况。

图6. 免疫荧光显微镜分析AgE6-DC表面展示(二)
诱导后3小时收获细胞。pEV,空载体菌株;cyt,胞内表达载体菌株;lipo、cwa2和LysM,携带不同表面锚定表达质粒的菌株。结果显示清酒乳杆菌、鼠李糖乳杆菌、弯曲乳杆菌和短乳杆菌的表面展示情况。
对于脂蛋白锚定的AgE6,结果变化更大。流式细胞术和荧光显微镜均显示嗜酸乳杆菌、清酒乳杆菌、鼠李糖乳杆菌和弯曲乳杆菌无或仅极弱信号,而其他四种菌株则有明显信号。这些变化可能表明表面展示蛋白的数量差异,但也可能反映抗原实际暴露程度的差异。细菌的肽聚糖层在组成、厚度和孔隙率上存在较大差异,这可能显著影响膜锚定靶蛋白的表面暴露程度和突出性。
显微镜分析显示,对所有乳杆菌菌株,膜锚定抗原的信号比细胞壁锚定抗原弱。这支持了细胞壁锚定抗原更易于抗体检测的观点。有趣的是,荧光显微镜还显示细胞内信号存在异质性,表明抗原分布不均匀。对于表达脂蛋白和LPXTG锚定抗原的细胞尤为明显。对于LPXTG锚定,已有研究表明细胞分裂调控与蛋白锚定密切相关。一些LPXTG锚定蛋白在细菌生长过程中迅速出现并聚集在隔膜处,而另一些则聚集在细胞壁较老的极区。观察到的异质性可能是由于所用信号肽或锚定序列中存在的细胞定位信号与细胞生长阶段变化的组合效应。
虽然本研究表明植物乳杆菌的锚定信号在多种乳杆菌物种中具有功能,但仍存在进一步优化的空间,例如使用同源锚定信号。值得注意的是,乳杆菌中指导分选酶介导锚定的LPXTG基序存在显著的物种特异性变异。虽然几种乳杆菌确实显示LPXTG共有序列,但植物乳杆菌的共有基序是LPQTXE,本研究中使用的基序是LPQTSE。这种特定的锚定基序可能与所有测试乳杆菌物种的分选酶系统兼容性不同。这可能部分解释了表达细胞壁锚定抗原的各种菌株生长特性的差异,也可能是抗原数量差异的一个因素。分选酶系统功能的变异也可能有助于解释表面展示抗原在细胞间和细胞内分布的观察到的变异。
在pSIP质粒中,编码启动子、靶蛋白、信号肽和锚定序列的片段通过带有酶切位点的连接子分隔,便于不同部分的交换。考虑到难以预测载体设计的成功,这种类似卡带的结构允许快速筛选多种设置,是有益的。
本研究系统评估了源自植物乳杆菌WCFS1的三种表面锚定序列在八种乳杆菌属物种中展示异源蛋白的效果。主要发现如下:
- LPXTG和LysM细胞壁锚定:在除嗜酸乳杆菌外的所有测试菌株中均成功实现表面展示,流式细胞术和荧光显微镜检测到明显信号。
- 脂蛋白锚定:效果变化较大,在植物乳杆菌、加氏乳杆菌、罗伊氏乳杆菌和短乳杆菌中成功,但在其他四种菌株中信号微弱或无信号。
- 不同乳杆菌物种在抗原生产水平、表面展示效率和生长受影响程度上存在显著差异。
- 流式细胞术和显微镜均观察到抗原展示的异质性,可能与细胞生长阶段和锚定蛋白的定位机制有关。
应用价值
本研究表明,源自植物乳杆菌的表面锚定序列是其他乳杆菌物种中异源蛋白锚定的有前景的候选工具。各种重组菌株在不同锚定方式下显示出不同效力的表面展示抗原。所有八种测试乳杆菌中有七种至少能通过三种测试锚定方式之一成功展示AgE6杂交分枝杆菌抗原。对于植物乳杆菌、加氏乳杆菌、罗伊氏乳杆菌和短乳杆菌,三种锚定策略均有效。这一研究成果为开发基于乳杆菌的口服疫苗和药物递送系统提供了重要的技术基础和筛选依据。通过选择合适的锚定策略和宿主菌株,可以优化抗原的表面展示,为后续免疫效果研究奠定基础。
主要参考文献:
[1] Duar RM, et al. Lifestyles in transition: evolution and natural history of the genus Lactobacillus. FEMS Microbiol Rev. 2017; 41: S27-S48.
[2] Wyszynska A, et al. Lactic acid bacteria-20 years exploring their potential as live vectors for mucosal vaccination. Appl Microbiol Biotechnol. 2015; 99: 2967-2977.
[3] Mohamadzadeh M, et al. Lactobacilli activate human dendritic cells that skew T cells toward T helper 1 polarization. Proc Natl Acad Sci USA. 2005; 102: 2880.
[4] Lebeer S, et al. Host interactions of probiotic bacterial surface molecules: comparison with commensals and pathogens. Nat Rev Microbiol. 2010; 8: 171.
[5] Michon C, et al. Display of recombinant proteins at the surface of lactic acid bacteria: strategies and applications. Microb Cell Fact. 2016; 15: 1-16.
[6] Kuczkowska K, et al. Immunogenic properties of Lactobacillus plantarum producing surface-displayed Mycobacterium tuberculosis antigens. Appl Environ Microbiol. 2017; 83.
[7] Kuczkowska K, et al. Comparison of eight Lactobacillus species for delivery of surface-displayed mycobacterial antigen. Vaccine. 2019; 37: 6371-6379.
[8] Mathiesen G, et al. Genome-wide analysis of signal peptide functionality in Lactobacillus plantarum WCFS1. BMC Genomics. 2009; 10:425.
[9] Karlskås IL, et al. Heterologous protein secretion in Lactobacilli with modified pSIP vectors. PLoS One. 2014; 9: e91125.
[10] Visweswaran G, et al. Exploiting the peptidoglycan-binding motif, LysM, for medical and industrial applications. Appl Microbiol Biotechnol. 2014; 98:4331-4345.
